- Nyitólap
- »
- Tudástár
Tudástár
REACH
Gyors, szakszerű regisztráció minimális költségen!
A REACH regisztráció sokkal komplexebb, mint ahogy elsőre gondoltuk; jó tanácsadó, vagy rendszeres REACH konferenciára járás nélkül bátor döntés megcsinálni egyedül a mini regisztrációs dossziét.
Az alábbi prezentációt ha megnézi, akkor a legegyszerűbb kérdéseire biztosan választ kap a REACH regisztrációval kapcsolatosan.
Ha még maradtak kérdései, kérem, nézze meg a REACH menüpontban az ide vonatkozó részt.

Ha tanácsadónak a cégemet választja, akkor 100% garanciát vállalok arra, hogy elsőre át fog menni a regisztrációs dosszié és nem fogják visszadobni. Ha nem így lesz, természetesen pénz visszatérítési-garanciát vállalok.
Mit csináljak, ha az általam érintett (PRE)-SIEF-ben még nincs vezető regisztráló?
Minél előbb derítse ki, hogy van- e vezető regisztráló, mert valakinek lenni kell, ez általában közös érdek. Az alábbi prezentációt ha megnézi, választ fog kapni arra, hogy hogyan derítse ki, hogy ki a vezető regisztráló az önök által gyártott vagy importált anyag esetében.
Ha az ön cége európai gyártó, és úgy tűnik, senki nem akarja elvállalni a vezető regisztráló szerepét, akkor ezt gyorsan jelentse a vezetőségnek, mert még az is megeshet, hogy Önöknek kell vállalni ezt a szerepet, ha senki más nem érintett ennek az adott anyag gyártásában 2018-ban. Ha a cége a vezető regisztráló, ez elég nagy anyagi megterheléssel jár, és erről a vezetőségnek időben tudnia kell.
Ha a vezető dosszié elkészítésre a cégemet választja, akkor erről előtte személyesen kell beszélnünk, ugyanis ez egy kb. 6-18 hónapos közös munkát jelent.
Ha az Ön vevője az Ön vegyi anyagából egy másik vegyi anyagot gyárt, akkor jó esélye van az olcsóbb intermedier regisztrációra. A REACH szerint az intermediernek nem kell minden esetben a telephelyen belül maradnia, tehát könnyen megeshet, hogy az Ön végterméke egy intermedier a REACH szerint.
Az anyag akkor intermedier, ha az összes következő feltétel teljesül:
- Az anyagot azért gyártották, hogy azt másik anyaggá alakítsák egy ipari telephelyen.
- A kémiai feldolgozás kimenete egy másik gyártott anyag önmagában, de nem egy másik anyag egy árucikkben
Az intermedier regisztráció nagyságrendekkel olcsóbb, mint a normál vegyi anyag regisztráció.
Az alábbi prezentációt ha megnézi, akkor a legegyszerűbb kérdéseire biztosan választ kap az intermedier regisztrációval kapcsolatosan.
Ha még maradtak kérdései, kérem, nézze meg a REACH menüpontban az ide vonatkozó részt, vagy keressen telefonon.

Ha tanácsadónak a cégemet választja, akkor 100% garanciát vállalok arra, hogy elsőre át fog menni a regisztrációs dosszié és nem fogják visszadobni. Ha nem így lesz, természetesen pénz visszatérítési-garanciát vállalok.
Vezető regisztráló dosszié elkészítése
Ne várjon arra, hogy egy másik cég legyen a vezető regisztráló, legyen az Ön cége, aki kontrollálja az árakat, legyen Ön a vezető regisztráló! Ezzel sok pénzt tud megtakarítani a cégének!
Az alábbi prezentációt ha megnézi, akkor a legegyszerűbb kérdéseire biztosan választ kap a REACH vezető regisztrációval kapcsolatosan.
Ha még maradtak kérdései, kérem, nézze meg a REACH menüpontban az ide vonatkozó részt.

Ha tanácsadónak a cégemet választja, akkor 100% garanciát vállalok arra, hogy elsőre át fog menni a regisztrációs dosszié és nem fogják visszadobni. Ha nem így lesz, természetesen pénz visszatérítési-garanciát vállalok.
Ha Ön új vegyi anyag felelős a cégénél, akkor magabiztosabban tudja ellátni a munkáját, ha kap egy alapos REACH és CLP oktatást vagy megrendel egy REACH auditot.
Az alábbi prezentációt ha megnézi, akkor a legegyszerűbb kérdéseire biztosan választ kap a kémiai biztonsági oktatásokkal kapcsolatosan.
Ha még maradtak kérdései, kérem, nézze meg a REACH menüpontban az ide vonatkozó részt.
CLP
A CLP egy EU rendelet, ami az EU „legerősebb”, kötelező jogszabályfajtája: minden tagországra általánosan érvényes, anélkül, hogy a nemzeti jogba külön át kellene emelni, és szóról szóra ugyanúgy kell lefordítani minden EU tagállamban.
Az Európai Parlament és Tanács vegyi anyagok és keverékek osztályozásáról, címkézéséről és csomagolásáról szóló 1272/2008/EK rendelete (Classification Labeling Packaging – CLP) 2009. január 20-án lépett hatályba, és egy átmeneti időszakot követően a jelenleg érvényben lévő osztályozási, címkézési és csomagolási irányelvek (67/548/EGK (DSD) és 1999/45/EK (DPD), Magyarországon 44/2000 EüM rendelet) helyébe lép. A CLP-rendeletet anyagokra 2010. december 1-jétől, keverékekre pedig 2015. június 1-jétől kell alkalmazni.
A magyar nyelvű CLP rendelet letöltése »
GHS prezentáció, 2010. május 6. – Securex kiállítás »
Hogyan tudja segíteni az Ön munkáját ezzel kapcsolatban a GHS-expert Kft. szoftveres szolgáltatása?
- Könnyen elérhető, professzionális CLP (GHS) osztályozás és címkézés a GHS-expert szoftver segítségével – azoknak, akik saját maguk akarnak osztályozni.
- Teljes körű osztályozás és címkézés a GHS-expert Kft. segítségével.
- Osztályozás bejelentése a GHS-expert Kft. segítségével.
Az Egyesült Nemzetek Szervezetének (ENSZ) keretében 12 év alatt gondosan kidolgozták az osztályozás és címkézés harmonizált kritériumait, valamint azok alkalmazásának általános elveit, aminek eredményeként létrejött a “Vegyi anyagok osztályozásának és címkézésének egyetemes harmonizált rendszere” a GHS (Global Harmonisation System). A CLP-rendelet nem más, mint a nemzetközileg elfogadott GHS-kritériumoknak az EU közösségi jogszabályokba való beépítése.
Az Európai Unión kívül egyre több ország fogadja el jogszabályaiban a GHS- kritériumokat.
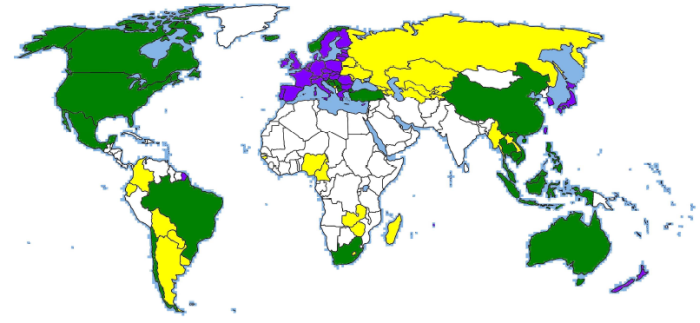
(lila: bevezetés alatt | zöld: bevezetése előkészületben | sárga: tárgyalás alatt)
A CLP rendelet célja
- A CLP egyik fő célja annak meghatározása, hogy az anyag vagy keverék rendelkezik-e olyan tulajdonságokkal, amelyek veszélyesként való besorolásához vezetnek. Ezt hívjuk osztályozásnak.Az osztályozási követelmények forgalmazott anyagokra, keverékekre, robbanóképes és pirotechnikai árucikkekre vonatkoznak függetlenül attól, hogy mekkora mennyiségben gyártották, importálták és forgalmazták az adott anyagot. 1t/év gyártott vagy importált mennyiség alatt is van osztályozási kötelezettség.Nem forgalmazott anyagokra is vonatkozik az osztályba sorolás, de csak amelyekre a REACH rendelet regisztrálást és bejelentést követel: pl.monomerek, elkülönített intermedierek, szállított elkülönített intermedierek, PPORD anyagok.
- Veszélyes anyagok és keverékek címkézésének harmonizálása .
Címkézési és csomagolási követelmények veszélyes anyagokra és készítményekre vonatkoznak. - Veszélyes anyagok és keverékek csomagolásának harmonizálása.
Az alábbi felsorolásban a CLP rendelethez tartozó jogszabályok, útmutatók, és hasznos linkeket talál, melyek segítségül szolgálnak Önnek.
Anyagok bejelentése az osztályozási és címkézési jegyzékbe »
A CLP rendelet bevezető útmutatója »
Útmutató az 1272/2008/EK rendelet szerinti címkézéshez és csomagoláshoz »
Helyesbítés az anyagok és keverékek osztályozásáról, címkézéséről és csomagolásáról »
Útmutató a biztonsági adatlapok elkészítéséhez »
(Felhívjuk a figyelmet, hogy egyes magyar nyelvű útmutatók az eredetileg angolul készült dokumentumoknak csak munkafordításai. A fordítást és a szerkesztési lektorálást az Európai Unió Szerveinek Fordítóközpontja végezte. A munkafordítások tudományos/technikai felülvizsgálatra fognak kerülni. Kizárólag az ECHA weboldalán is hozzáférhető angol nyelvű változatok az eredetiek.)
- Radioaktív anyagok
- Vámszabad területen lévő anyagok, Tranzitáruk,
- Nem elkülönített intermedierek
- Kutatás – fejlesztési anyagok (feltételekkel)
- Hulladékok
- Honvédelem esetén (feltételekkel)
- Gyógyszerek, Állatgyógyászati készítmények
- Kozmetikai termékek
- Orvostechnikai eszközök
- Élelmiszerek és Takarmányok
További információkért kérjük, töltse le a CLP rendelet teljes szövegét »
Az új CLP (GHS) piktogramokat az ábrák alatti linkekre kattintva tudja .gif, .eps vagy .tif formátumban letölteni. Ha nem tudja, melyik a megfelelő formátum az Ön számára, kérje ki a nyomdai munkálatokkal megbízott szakember véleményét.
Az új piktogramok alatt Ön a régi veszélyszimbólum ábrákat is megtalálja. Tudnia kell azonban, hogy a vegyi anyag vagy készítmény címkéjén tilos együtt használni a régi és az új piktogramokat!
Új veszélyszimbólumok
Régi veszélyszimbólumok

Figyelem! A vegyi anyag vagy készítmény címkéjén tilos a régi és az új piktogramokat együtt használni!
A gyártónak, importőrnek, továbbfelhasználónak (beleértve a készítőt is) vagy forgalmazónak (beleértve a kiskereskedőt is), a forgalomba hozatalt megelőzően címkéznie kell valamennyi veszélyes anyagot vagy keveréket (a CLP 4. cikkének (4) bekezdése).
Ez vonatkozik az olyan árucikkek előállítóira és importőreire is, amelyek a CLP I. mellékletének 2. részében levő kritériumok szerint robbanóképesek.
A forgalmazónak, a címkézés céljaira nem kell az osztályba sorolást elölről kezdenie, hanem átveheti szállítójától az anyag vagy a keverék osztályozását. Ugyanez a szabály érvényes a továbbfelhasználóra is, feltéve, hogy nem változtatja meg a neki szállított anyag vagy keverék összetételét.
A címkéit azon tagállam(ok) hivatalos nyelvén (nyelvein) kell megfogalmazni, amely(ek)ben az anyagot vagy keveréket forgalomba hozzák, kivéve, ha az érintett tagállam(ok) másként nem rendelkezik (rendelkeznek). Ebben a vonatkozásban szükséges lehet a vonatkozó nemzeti szabályozás ezen előírásainak ellenőrzése. Több nyelvű címke lehetséges.
Címke minimális tartalma
- Szállító neve, címe, telefonszáma
- Mennyiség
- Termékaznosítók ( CAS#, EC#, IUPAC név)
- Veszélyt jelző piktogramok
- Figyelmezetések (Veszély, Figyelem)
- Figyelmeztető mondatok
- Óvintézkedésre vonatkozó mondatok
- Kiegészítő információs mező (biocid, engedélyszám)

Címke és piktogram méretei
(Eltérés speciális esetekben lehetséges)
| A csomag űrtartalma | Címke méretek (mm) | Piktogram méretek (mm) |
| Legfeljebb 3 liter | Ha lehet legalább 52×74 | Legalább 16×16 |
| 3 liternél nagyobb, de legfeljebb 50 liter | Legalább 74×105 | Legalább 23×23 |
| 50 liternél nagyobb, de legfeljebb 500 liter | Legalább 105×148 | Legalább 32×32 |
| 500 liternél nagyobb | Legalább 148×210 | Legalább 45×45 |
Felhasznált irodalom
A CLP-rendelet (A CLP az anyagok és keverékek osztályozásáról, címkézéséről és csomagolásáról szóló 1272/2008/EK rendelet)
A CLP-rendelet bevezető útmutatója »
Kérdése van?
Amennyiben további kérdései vannak kérjük, vegye fel velünk a kapcsolatot az alábbi elérhetőségeinken:
Botos Ágnes
A GHS-expert Kft. ügyvezetője
E-mail: agnes.botos@ghsexpert.com
Telefon: +36-20/220-5737
A CLP-rendelet 2009. január 20-án lépett hatályba. Mindazonáltal nem azonnal kötelező érvényű a CLP-rendelet valamennyi rendelkezése: a CLP 61. cikkében lefektetett átmeneti rendelkezések a veszélyes anyagok és keverékek osztályozására, a veszélyesség közlésére és a csomagolásukra két határidőt tűznek ki, nevezetesen 2010. december 1. anyagok esetében és 2015. június 1. napját keverékek esetében.
Az alábbi táblázat segít a rendelet határidejének értelmezésében. Mivel nagyon fontos megérteni ezeket a határidőket, az útmutató ide vonatkozó részét is feltettem a honlapomra.
| időszak | Vegyi termék | Osztályozás∗∗ | Bejelentés | Biztonsági adatlap∗∗∗ | Címkézés és csomagolás∗ |
| 2009.01.20 – 2010.11.30 | Anyag | 44/2000 | 44/2000 vagy CLP | 44/2000 | 44/2000 |
| vagy 44/2000 és CLP | 44/2000 vagy CLP | 44/2000 és CLP | CLP | ||
| Keverék | 44/2000 | – | 44/2000 | 44/2000 | |
| vagy 44/2000 és CLP | – | 44/2000 és CLP | CLP | ||
| 2010.12.01 – 2015.05.31 | Anyag | 44/2000 és CLP | CLP | 44/2000 és CLP | CLP |
| Keverék | 44/2000 | – | 44/2000 | 44/2000 | |
| vagy 44/2000 és CLP | – | 44/2000 és CLP | CLP | ||
| 2015.06.01 – től | Anyag | CLP | CLP | CLP | CLP |
| Keverék | CLP | – | CLP | – |
*Azon anyagokat amelyek a 44/2000 EüM. rendelet szerint osztályoztak, címkéztek és csomagoltak, és 2010. december 1. előtt már forgalomba hoztak, 2012.dec .1-jéig nem szükséges a CLP szerint újracímkézni és csomagolni.
*Azon keverékeket amelyek a 44/2000 EüM. rendelet szerinti osztályoztak, címkéztek és csomagoltak, és 2015. június 1. előtt már forgalomba hoztak, 2017.jún.1-jéig nem szükséges a CLP szerint újracímkézni és csomagolni.
**44/2000 EüM. rendelet harmonizál a 67/548/EEC Dangerous Substance Directive, „DSD” –vel és a 1999/45/EC, Dangerous Preparations Directive, „DPD” –vel.
***Biztonsági adatlapot akkor kell kiadni, ha a felsorolt szabályozások szerint veszélyes a termékünk, és az ezek szerinti osztályozást kell oda beleírni, mindig melléírva, hogy az harmonizált, vagy saját osztályozás-e.
2009. január 20-tól a következő szabályok lépnek életbe
- 2010. december 1-ig az anyagokat továbbra is a 44/2000 Eüm. rendelet szerint kell osztályozni, címkézni és csomagolni. Azonban már ezen időpont előtt is lehetséges az anyagok CLP szerinti osztályozása, címkézése és csomagolása. Ha erre kerül sor, akkor a 44/2000 Eüm. rendelet címkézési és csomagolási előírásai már nem alkalmazandók az anyagra. Ez azt jelenti, hogy a címkézésnek és a csomagolásnak a CLP rendelkezéseire kell figyelemmel lennie;
- 2015. június 1-ig a keverékeket továbbra is a 44/2000 Eüm. rendelet szerint kell osztályozni, címkézni és csomagolni. Azonban már ezen időpont előtt is lehetséges a keverékek CLP szerinti osztályozása, címkézése és csomagolása. Ha erre kerül sor, akkor a 44/2000 Eüm. rendelet címkézési és csomagolási előírásai már nem alkalmazandók a keverékre. Ez azt jelenti, hogy a címkézésnek és a csomagolásnak a CLP rendelkezéseire kell figyelemmel lennie;
- 2015. június 1-jéig fel kell tüntetni az anyagok 44/2000 Eüm. rendelet szerinti osztályozását a biztonsági adatlapon. Ez vonatkozik maguknak az anyagoknak a biztonsági adatlapjára, és az ezen anyagokat tartalmazó keverékek biztonsági adatlapjára is;
- 2010. december 1-jéig, ha az anyag osztályozása, címkézése és csomagolása a CLP szerint történt, akkor a CLP osztályozást kötelező feltüntetni a biztonsági adatlapon a 44/2000 Eüm. rendelet szerinti osztályozás mellett. A szállító azonban már azelőtt választhatja valamely anyag CLP szerinti osztályozáson alapuló azonosítását, mielőtt a CLP-t teljes egészében alkalmazná. Amennyiben erre kerül sor, a szállító feltüntetheti ezt az információt a kísérő biztonsági adatlapon az „egyéb információ” fejléc alatt;
- 2015. június 1-jéig a keverék 44/2000 Eüm. rendelet szerinti osztályozását kötelező feltüntetni a biztonsági adatlapon;
- 2015. június 1-jéig, ha a keverék osztályozása, címkézése és csomagolása a CLP szerint történt, akkor a CLP osztályozást kötelező feltüntetni a biztonsági adatlapon a 44/2000 Eüm. rendelet szerinti osztályozás mellett. A szállító azonban már azelőtt választhatja valamely keverék CLP szerinti osztályozáson alapuló azonosítását, mielőtt a CLP-t teljes egészében alkalmazná. Amennyiben erre kerül sor, a szállító feltüntetheti ezt az információt a kísérő biztonsági adatlapon az „egyéb információ” fejléc alatt;
- 2009. január 20-ától megkezdődik az V. cím alkalmazása, a gyártók, importőrök és továbbfelhasználók benyújthatják a harmonizált osztályozásra vonatkozó javaslataikat az Ügynökségnek (a CLP 37. cikkének (2) bekezdése),valamint be kell nyújtaniuk a javaslatukat a tagállam illetékes hatóságához abban az esetben, ha olyan új információ jutott tudomásukra, amely a harmonizált osztályozás és címkézés megváltozásához vezethet (a CLP 37. cikkének (6) bekezdése).
2010. december 1-jén a következő szabályok lépnek életbe
- Az anyagokat kötelező a 44/2000 Eüm. rendelet és a CLP szerint is osztályozni;
- Az anyagokat kizárólag a CLP szerint kötelező címkézni és csomagolni, de a 44/2000 Eüm. rendelet szerint már osztályozott, címkézett, csomagolt és 2010. december 1. előtt forgalomba helyezett (vagyis a „polcokon lévő”) anyagokat csak 2012. december 1-jéig kell átcímkézni és átcsomagolni;
- 2015. június 1-jéig a keverékeket továbbra is a 44/2000 Eüm. rendelet szerint kell osztályozni, címkézni és csomagolni. Azonban már ezen időpont előtt is lehetséges a keverékek CLP szerinti osztályozása, címkézése és csomagolása. Ha erre kerül sor, akkor a 44/2000 Eüm. rendelet címkézési és csomagolási előírásai már nem alkalmazandók a keverékre. Ez azt jelenti, hogy a címkézésnek és a csomagolásnak figyelemmel kell lennie a CLP rendelkezéseire;
- 2015. június 1-jéig az anyagok 44/2000 Eüm. rendelet szerinti osztályozását kötelező feltüntetni a biztonsági adatlapon a CLP osztályozás mellett. Ez vonatkozik maguknak az anyagoknak a biztonsági adatlapjára, és az ezeket az anyagokat tartalmazó keverékek biztonsági adatlapjára is;
- 2015. június 1-jéig, a keverék 44/2000 Eüm. rendelet szerinti osztályozását kötelező feltüntetni a biztonsági adatlapon;
- 2015. június 1-jéig, ha a keverék osztályozása, címkézése és csomagolása a CLP szerint történt, akkor a CLP osztályozást kötelező feltüntetni a biztonsági
- Adatlapon a 44/2000 Eüm. rendelet szerinti osztályozás mellett. A szállító azonban már azelőtt választhatja valamely keverék CLP szerinti osztályozáson alapuló azonosítását, mielőtt a CLP-t teljes egészében alkalmazná. Amennyiben erre kerül sor, a szállító feltüntetheti ezt az információt a kísérő biztonsági adatlapon az „egyéb információ” fejléc alatt.
2015. június 1-jét a következő szabályok lépnek életbe
- Az anyagokat kizárólag a CLP szerint kötelező osztályozni;
- A keverékeket kizárólag a CLP szerint kötelező osztályozni, címkézni és csomagolni, de a 44/2000 Eüm. rendelet szerint már osztályozott, címkézett, csomagolt és 2015. június 1. előtt forgalomba helyezett (vagyis a „polcokon lévő”) anyagokat csak 2017. június 1-jéig kell átcímkézni és átcsomagolni; és
- Az anyagok és keverék CLP szerinti osztályozását kötelező feltüntetni a biztonsági adatlapon.
Az osztályozási követelmények forgalmazott anyagokra, keverékekre, robbanóképes és pirotechnikai árucikkekre vonatkoznak.
1t/év gyártott vagy importált mennyiség alatt is van osztályozási kötelezettség.
Nem forgalmazott anyagokra is vonatkozik az osztályba sorolás, de csak amelyekre a REACH rendelet regisztrálást és bejelentést követel: pl. elkülönített intermedierre.
A CLP kétféle típusú osztályozást tartalmaz: a saját osztályozást és a harmonizált osztályozást.
Az anyagok harmonizált osztályozása
Az anyagok harmonizált osztályozását a CLP VI. mellékletének 3.1. táblázata tartalmazza (több ezer anyag). A harmonizált osztályozástól eltérni nem lehet, a gyártók és importőrök kötelesek ezt az osztályozást alkalmazni. Tagállamok hatóságai valamint az ipar is javasolhat új anyagokat a Harmonizált Osztályozási jegyzékbe, így a CLP VI. mellékletének 3.1 táblázat frissülni fog a jövőben, amennyiben a Bizottság további harmonizált osztályozásokról dönt.
A megfelelési táblázatok
Az osztályozással kapcsolatosan el kell döntenie azt is, hogy milyen mértékben kívánja felhasználni a CLP VII. mellékletében rendelkezésre bocsátott megfelelési táblázatokat, amelyek a régi osztályozásokat feleltetik meg a CLP osztályozásoknak. A megfelelési táblázatból közvetlen megfeleltetés nem lehetséges legtöbb esetben.
Ha egy anyag harmonizált osztályozású és ennek megfelelően a CLP VI. mellékletében található táblázatokban szerepel, akkor nem szükséges az adott veszélyre vonatkozóan rendelkezésre álló információt összegyűjtenie erről az anyagról. Más szavakkal: az információgyűjtés megkezdése előtt először a VI. mellékletet kell átnéznie.
Ha egy vegyi anyag nincs rajta a Harmonizált Osztályozási jegyzéken, akkor a VII. melléklet megfelelési táblázata és az I. melléklet besorolási és címkézési előírása szerint kell osztályozni.
A veszélyességi információk
A kapott veszélyességi információk megfelelésének és megbízhatóságának eldöntésekor meg kell fontolnia, hogy rendelkezik-e elegendő szakértelemmel. Ha nem, akkor szakértővel kell konzultálnia. Önnek vagy a bevont szakértőnek meg kell bizonyosodnia arról, hogy az összegyűjtött információ az osztályozás céljára megfelelő és megbízható.
Az információnak az anyag azon formájára vagy fizikai állapotára kell vonatkoznia, amelyben az anyagot forgalomba hozzák, és amelyben ésszerűen feltételezhető, hogy használni fogják.
A fizikai veszélyek tekintetében új információt kell létrehozni az osztályozáshoz és a címkézéshez, hacsak nem áll rendelkezésre megfelelő és megbízható információ. Mindazonáltal az egészségi és környezeti veszélyek tekintetében nem kötelező a vizsgálatok elvégzése.
A korábban veszélyesnek nem minősülő anyagok vagy keverékek a CLP szerint veszélyesnek minősülhetnek.
A keverékek osztályozása
A keverékek CLP szerinti osztályozása ugyanazon veszélyek tekintetében történik, mint az anyagok osztályozása. Az anyagokkal egyező módon, a keverékekről rendelkezésre álló adatokat elsődlegesen teljes egészükben kell figyelembe venni az osztályozás megállapításakor.
Ha erre nincs lehetőség, akkor a keverékek osztályozásához olyan további megközelítéseket lehet alkalmazni, mint például „interpolációs elvek” a hasonló vizsgált keverékekre és az egyes veszélyes összetevő anyagokra vonatkozó, rendelkezésre álló adatok felhasználásával.
Fizikai veszélyek
Robbanóanyagok
Inst. robb.
Robb. 1.1
Robb. 1.2
Robb. 1.3
Robb. 1.4
Robb. 1.5
Robb. 1.6
Tűzveszélyes gázok
Tűzv. gáz 1
Tűzv. gáz 2
Tűzveszélyes aeroszolok
Tűzv. aeroszol 1
Tűzv. aeroszol 2
Oxidáló gázok
Oxid. gáz 1
Nyomás alatt lévő gázok
Nyom. alatt lévő gáz (*)
Tűzveszélyes folyadékok
Tűzv. foly. 1
Tűzv. foly. 2
Tűzv. foly. 3
Tűzveszélyes szilárd anyagok
Tűzv. szil. 1
Tűzv. szil. 2
Önreaktív anyagok és keverékek
Önreakt. A
Önreakt. B
Önreakt. CD
Önreakt. EF
Önreakt. G
Öngyulladó folyadékok = Piroforos folyadékok
Öngyull. foly. 1
Öngyulladó szilárd anyagok = Piroforos szilárd anyagok
Öngyull. szil. 1
Önmelegedő anyagok és keverékek
Önm. 1
Önm. 2
Vízzel érintkezve tűzveszélyes gázokat kibocsátó anyagok és keverékek
Vízzel ér. 1
Vízzel ér. 2
Vízzel ér. 3
Oxidáló folyadékok
Ox. foly. 1
Ox. foly. 2
Ox. foly. 3
Oxidáló szilárd anyagok
Ox. szil. 1
Ox. szil. 2
Ox. szil. 3
Szerves peroxidok
Szerv. perox. A
Szerv. perox. B
Szerv. perox. CD
Szerv. perox. EF
Szerv. perox. G
Fémekre maró hatású anyagok és keverékek = Fémekre korrozív hatású anyagok
Fémre maró 1 = Fémre korrozív 1
Egészségi veszélyek
Akut toxicitás
Akut tox. 1
Akut tox. 2
Akut tox. 3
Akut tox. 4
Bőrmarás/bőrirritáció
Bőrmaró 1A
Bőrmaró 1B
Bőrmaró 1C
Bőrirrit. 2
Súlyos szemkárosodás/szemirritáció
Szemkár. 1
Szemirrit. 2
Légzőszervi/bőr szenzibilizáció
Légz. szenz. 1
Bőrszenz. 1
Csírasejt-mutagenitás
Muta. 1A
Muta. 1B
Muta. 2
Rákkeltő hatás
Rákk. 1A
Rákk. 1B
Rákk. 2
Reprodukciós toxicitás
Repr. 1A
Repr. 1B
Repr. 2
Lakt.(laktáció)
Célszervi toxicitás – egyszeri expozíció
STOT egy. 1
STOT egy. 2
STOT egy. 3
Célszervi toxicitás – ismétlődő expozíció
STOT ism. 1
STOT ism. 2
Aspirációs veszély
Asp. vesz. 1
Környezeti veszélyek
A vízi környezetre veszélyes
Vízi, akut 1
Vízi, krónikus 1
Vízi, krónikus 2
Vízi, krónikus 3
Vízi, krónikus 4
Az ózonrétegre veszélyes
Ózon
Anyagok gyártójaként, anyagok vagy keverékek importőreként vagy továbbfelhasználóként össze kell állítania és elérhetővé kell tennie azon információkat, amelyeket az anyaga vagy keveréke osztályozásához és címkézéséhez felhasznált. Ezt az információt az anyag vagy keverék utolsó szállítása után legalább tíz évig meg kell őrizni (a CLP 49. cikke).
A székhelye szerinti tagállam illetékes hatósága(i), végrehajtásért felelős hatósága vagy az Ügynökség felszólíthatják, hogy nyújtson be minden információt, amit a CLP szerinti osztályozáshoz és címkézéshez használt. Egy ilyen megkeresés alapján rendelkezésre kell bocsátania ezt az információt.
Példa:
Nátrium-metaszilikát osztályozása EC#: 229-912-9
GHS VI. melléklet 3.1 táblázat: Harmonizált Osztályozási jegyzék
| CLP bejelentés jogi személyként | |||
| Besorolás | Címkézés | ||
| Veszélyességi osztályok és kategóriák kódjai | Figyelmeztető mondatok kódjai | Kiegészítő figyelmeztető mondatok kódjai | Figyelmeztető mondatok kódjai |
| Skin Corr. 1 B | H314 | GHS05 | H314 |
| STOT SE 3 | H335 | GHS0 | H335 |
| Dgr | |||
Címkézési segédtáblázat
| Bőrmarásra vonatkozó címkeelemek /Skin Corr. 1 B/ | Célszervi toxicitás (egyszeri expozíció) /STOT SE 3/ | ||
| Besorolás | 1. kategória B/1 | ||
| GHS piktogram |  |
 |
|
| Figyelmeztetés | Veszély | Figyelem | |
| R – mondat | Figyelmeztető mondat | H314: Súlyos égési sérülést és szemkárosodást okoz. | H335:Légúti irritációt okozhat |
| S – mondat | Óvintézkedésre vonatkozó mondat -Megelőzés | P260 | P261 |
| P264 | P271 | ||
| P280 | |||
| Óvintézkedésre vonatkozó mondat-Elhárító intézkedés | P301+P330+P331 | P304+P340 | |
| P303+P361+P353 | P312 | ||
| P363 | |||
| P304+P340 | |||
| P310 | |||
| P321 | |||
| P305+P351+P338 | |||
| Óvintézkedésre vonatkozó mondat – Tárolás | P405 | P403+P233 | |
| P405 | |||
| Óvintézkedésre vonatkozó mondat – Elhelyezés hulladékként | P501 | P50 |
A jelenlegi R-mondatokat, S-mondatokat a CLP figyelmeztető mondatokkal és óvintézkedésre vonatkozó mondatokkal helyettesíti.
Címkére írható szöveg: Óvintézkedésre vonatkozó mondatokból elég csak 6-ot ráírni.
Egy konkrét példa erre:

Az anyagot forgalomba hozó gyártó vagy importőr (vagy a gyártók vagy importőrök valamely csoportjának tagja) bizonyos információkat be kell jelentenie az Európai Vegyianyag-ügynökségnek (a CLP 40. cikke), amennyiben az anyaga:
- a REACH szerint regisztrálandó (≥ 1 tonna / év) és forgalomban van (a CLP 39. cikkének a) pontja). Kérjük, vegye figyelembe, hogy a REACH szerint már regisztrált anyagot nem kell ismét bejelentenie, amennyiben a bejelentendő információt már a regisztrálási dokumentáció részeként benyújtotta. Ez vonatkozik bizonyos, árucikkekben található anyagokra is, ha a REACH 7. cikke előírja regisztrációjukat.
- a CLP szerint veszélyesként besorolt és forgalomban van, mennyiségtől függetlenül (a CLP 39. cikkének b) pontja); vagy
- a CLP szerint veszélyesként besorolt és valamely keverékben a CLP I. mellékletében vagy a 44/2000 EüM. rendeletben meghatározott határértékeket meghaladó koncentrációban van jelen, aminek következtében a készítmény veszélyes készítményként osztályozandó, és a keverék forgalomban van (a CLP 39. cikkének b) pontja).
A bejelentés határideje
Ha Ön keveréket készítő tovább felhasználó, forgalmazó vagy árucikk előállító a REACH 7. cikke értelmében, akkor nem szükséges bejelentést tennie az Ügynökségnek. Ennek oka, hogy az anyagára vonatkozó bejelentés a szállítói lánc egy korábbi szakaszában már megtörténik.
A 2010. december 1. előtt forgalomba hozott, valamint a még vagy ismét forgalomban levő anyagok esetében a jegyzékbe való bejelentés határideje az innentől számított egy hónap, azaz 2011. január 1. Azonban, mivel január 1. szombatra, január 2. pedig vasárnapra esik, a bejelentési határidő a gyakorlatban 2011. január 3. A leendő bejelentők tartsák emlékezetükben, hogy 2010. december 24. és 2011. január 2. között hivatalos munkaszüneti időszak lesz az ECHA-nál. Ennek megfelelően azt javasoljuk, hogy – ha lehetséges – a bejelentést 2010. december 24. előtt nyújtsák be, ami lehetővé teszi bármely, a benyújtási eszközzel jelentkező műszaki probléma idejében történő megoldását, így csökkentve a sikeres bejelentés nehézségeinek kockázatát.
A 2010. december 1. után forgalomba kerülő anyagokra az egy hónapos időszakot onnantól kell számítani, amikor 2010. december 1-jét követően először forgalomba kerülnek.
Egy kitűnő példa:
Például gyártóként vagy importőrként 2010. november 8-án szállít egy anyagot, majd egy időre leállítja a szállítást, és azután 2011. február 1-jén ismét megkezdi azt. Az egy hónapos kötelező bejelentési határidőt 2011. február 1-től kell számolni, ezért a bejelentése legkésőbb március 1-jén esedékes. Természetesen, önkéntes alapon már 2010. december 1. előtt is megteheti bejelentését.
Kinek a feladata a bejelentés? Az anyag gyártóké és az importőröké.
Ha regisztrálja az anyagát a REACH szerint 2010. december 1-jéig, akkor a vezető regisztráló a regisztrációs dosszié megküldésével együtt a CLP (GHS) bejelentést is meg fogja tenni a cége helyett. Ez estben az Ön cégének nem kell külön CLP (GHS) bejelentést tenni.
Ha nem regisztrálja az anyagát a REACH szerint 2010. december 1-jéig, akkor be kell jelentenie azt 2011. január 1-jég.
A CLP VI. mellékletében a 3.1 táblázatban a Harmonizált Osztályozási Listában szereplő vegyi anyagokat is be kell jelenteni.
A bejelentési kötelezettséget összefoglaló táblázat:
| CLP bejelentés jogi személyenként | ||||||
| Anyag | Bejelentési határidő | Bejelentést végző | Kinek nem kell bejelenteni? | Tonna | Veszélyesség figyelembevétele | Forgalomba hozatal |
| REACH szerint 2010-ben regisztrálandó anyagok | 2010. dec. 1. | Vezető regisztráló | 2010-es regisztrálóknak, mert helyettük a vezető regisztráló készíti el a REACH regisztrációs dosszié részeként | 1 tonna felett | veszélyest és nem veszélyest is | számít |
| REACH szerint 2013-ban vagy 2018-ban regisztrálandó anyagok és forgalomban vannak | 2010. dec. 24. | 2013-as és 2018-as regisztrálók | (csoportos bejelentés résztvevőinek ?, REACH egyedüli képviselők (OR) helyett importőröknek kell bejelenteni?) | 1 tonna felett | veszélyest és nem veszélyest is | számít |
| REACH szerint 2013-ban vagy 2018-ban regisztrálandó anyagok és nincsenek forgalomban 2010. dec 1-jén | 2010. dec. 24. önkéntesen vagy 1 hónappal a forgalomba hozatal után | 2013-as és 2018-as regisztrálók | (csoportos bejelentés résztvevőinek ?, REACH egyedüli képviselők (OR) helyett importőröknek kell bejelenteni?) | 1 tonna felett | veszélyest és nem veszélyest is | számít |
| 2010. dec. 1. után forgalomba hozott veszélyes anyagok ha még REACH regisztrációban nem jelentették be (az import forgalomba hozatalnak számít) | 1 hónappal a forgalomba hozatal után | gyártó, importőr | – | bármilyen mennyiségnél | veszélyes | számít |
| 2010. dec. 1. után forgalomba hozott veszélyes készítmények megfelelő* komponensei (a veszélyes készítmény azon összetevői amelyek nem voltak REACH regisztrációban bejelentve | 1 hónappal a forgalomba hozatal után | gyártó, importőr | – | bármilyen mennyiségnél | veszélyest és nem veszélyest is | számít |
| 2010. dec. 1 után először gyártott vagy importált REACH szerint regisztrálandó anyagok ha még nem voltak REACH szerint regisztrálva | 1 hónappal a forgalomba hozatal után | gyártó, importőr | (REACH egyedüli képviselők(OR) helyett importőröknek kell bejelenteni?) | 1 tonna felett | veszélyest és nem veszélyest is | számít |
Bejelentési eszközök
- IUCLID 5.2 + REACH-IT
- Tömeges bejelentés XML fájl segítségével + REACH-IT
- REACH-IT on-line bejelentés
- REACH-IT Gyártók / importőrök csoportos bejelentése
Csoportos CLP (GHS) bejelentés
Legfrissebb információ: A CLP (GHS) bejelentést gyártók és importőrök csoportja is beadhatja, s ez nagy könnyebbség az ipar szereplőinek. Az Európai Vegyianyag-ügynökség most dolgozza ki a részleteket.
Készpénzt és időt érő tanácsok a CLP rendelettel kapcsolatosan, most Díjtalanul!
BIOCID
Hogyan is fogjon hozzá az új biocid rendelet betartásához az a cég, aki biocid hatóanyagot gyárt az EU-ban?
A legfontosabb szabály amire figyelnie kell:
2015. szeptember 1-jétől nem hozható forgalomba a biocid termék, amennyiben a benne lévő hatóanyag(ok) gyártója vagy importőre, illetve adott esetben a biocid termék importőre nem szerepel az alábbi listán:
Elfogadott hatóanyagok »
(Az ECHA rendszeresen aktualizálja ezt a listát)
Az első feladat:
- Mivel Önök biocid hatóanyagot gyártanka ezért 2015. szeptember 1-jére fel kell kerülniük az elfogadott hatóanyag listára. Ha nem kerülnek fel erre a listára, akkor 2015. szeptember 1-vel nem gyárthatják a biocid hatóanyagot, és nem is hozhatja az Önök által gyártott hatóanyagot tartalmazó biocid terméket senki sem forgalomba az EU-ban. Tehát van 2 évük, hogy kivezessék a piacról ezt a biocid hatóanyagot, és felkészítsék erre a jelenlegi vevőiket. Ha szeretnék, hogy felkerüljenek az elfogadott hatóanyagok listára, akkor az alábbi teendőjük van.
- Az R4BP rendszeren keresztül inquiry-t nyújtanak be, hogy megkapják a konkrét elérhetőségét azoknak a cégeknek, akiknek már vannak tesztjeik, és akiktől hozzáférési felhatalmazást (LOA) lehetne szerezni.Ha inquiry nélkül is meg tudják találni a lista alapján az elérhetőséget az lenne a leggyorsabb megoldás.
- Tárgyalnak a hozzáférési felhatalmazás (LOA) áráról vagy
- Saját maguk megcsináltatják / összegyűjtik a teszteket a II és III melléklet követelményei alapján. Ez egy hatalmas munka, jó biocid tanácsadó nélkül nem fogják tudni megcsinálni.
- Hatóanyag jóváhagyást nyújtanak be
Hatóanyag jóváhagyás
A biocid hatóanyag gyártójának vagy importőrének be kell adni a hatóság felé a 6. cikk alapján egy hatóanyag jóváhagyási IUCLID dosszié-t a R4BP rendszeren keresztül 2015. szeptember 1-ig, ami alapján felkerül a hatóanyag az elfogadott hatóanyagok listára.
Tartalma:
- a hatóanyagra vonatkozó dokumentációt (II. melléklet) vagy
- a hatóanyagra vonatkozó hozzáférési felhatalmazást (LOA) és
- a biocid termékre vonatkozó dokumentációt (III. melléklet) vagy
- a biocid termékre vonatkozó hozzáférési felhatalmazást (LOA).
Felülvizsgálati program
A hatóanyagot egy felülvizsgálati programon belül értékeli az EU Bizottsága az alábbi határidőre:
| Priority | Existing active substances for product types |
All draft CARs have to be submitted to ECHA by |
The BPC have to submit all its opinions by |
| 1st priority list | 8, 14, 16, 18, 19, 21 | 31/12/2015 | 31/12/2016 |
| 2nd priority list | 3, 4, 5 | 31/12/2016 | 31/12/2017 |
| 3rd priority list | 1, 2 | 31/12/2018 | 31/12/2019 |
| 4th priority list | 6, 13 | 31/12/2019 | 31/12/2020 |
| 5th priority list | 7, 9, 10 | 31/12/2020 | 31/12/2021 |
| 6th priority list | 11, 12, 15, 17, 22, 23 (new PT20 under BPR) |
31/12/2022 | 31/06/2024 |
Ha a hatóanyag felülvizsgálat sikeresen lezárul, akkor 5, 7. vagy 10 évig fennmaradhat a hatóanyag az elfogadott hatóanyagok listáján.
Hogyan is fogjon hozzá az új biocid rendelet betartásához az a cég, aki biocid hatóanyagot importál az EU-ba?
A legfontosabb szabály amire figyelnie kell:
2015. szeptember 1-jétől nem hozható forgalomba a biocid termék, amennyiben a benne lévő hatóanyag(ok) gyártója vagy importőre, illetve adott esetben a biocid termék importőre nem szerepel az alábbi listán:
Elfogadott hatóanyagok »
(Az ECHA rendszeresen aktualizálja ezt a listát)
Az első feladat:
- Mivel Önök biocid hatóanyagot importálnak az EU-n kívülről, ezért 2015. szeptember 1-jére fel kell kerülniük az elfogadott hatóanyag listára.
Ha nem kerülnek fel erre a listára, akkor 2015. szeptember 1-vel nem importálhatják a biocid hatóanyagot, és nem is hozhatja az Önök által gyártott hatóanyagot tartalmazó biocid terméket senki sem forgalomba az EU-ban. Tehát van 2 évük, hogy kivezessék a piacról ezt a biocid hatóanyagot, és felkészítsék erre a jelenlegi vevőiket.
Ha szeretnék, hogy felkerüljenek az elfogadott hatóanyagok listára, akkor az alábbi teendőjük van. - Az R4BP rendszeren keresztül inquiry-t nyújtanak be, hogy megkapják a konkrét elérhetőségét azoknak a cégeknek, akiknek már vannak tesztjeik, és akiktől hozzáférési felhatalmazást (LOA) lehetne szerezni.
Ha inquiry nélkül is meg tudják találni a lista alapján az elérhetőséget az lenne a leggyorsabb megoldás. - Tárgyalnak a hozzáférési felhatalmazás (LOA) áráról vagy
- Saját maguk megcsináltatják / összegyűjtik a teszteket a II és III melléklet követelményei alapján. Ez egy hatalmas munka, jó biocid tanácsadó nélkül nem fogják tudni megcsinálni.
- Hatóanyag jóváhagyást nyújtnak be.
Hatóanyag jóváhagyás
A biocid hatóanyag gyártójának vagy importőrének be kell adni a hatóság felé a 6. cikk alapján egy hatóanyag jóváhagyási IUCLID dosszié-t a R4BP rendszeren keresztül 2015. szeptember 1-ig, ami alapján felkerül a hatóanyag az elfogadott hatóanyagok listára.
Tartalma:
- a hatóanyagra vonatkozó dokumentációt (II. melléklet) vagy
- a hatóanyagra vonatkozó hozzáférési felhatalmazást (LOA) és
- a biocid termékre vonatkozó dokumentációt (III. melléklet) vagy
- a biocid termékre vonatkozó hozzáférési felhatalmazást (LOA).
Felülvizsgálati program
A hatóanyagot egy felülvizsgálati programon belül értékeli az EU Bizottsága az alábbi határidőre:
| Priority | Existing active substances for product types |
All draft CARs have to be submitted to ECHA by |
The BPC have to submit all its opinions by |
| 1st priority list | 8, 14, 16, 18, 19, 21 | 31/12/2015 | 31/12/2016 |
| 2nd priority list | 3, 4, 5 | 31/12/2016 | 31/12/2017 |
| 3rd priority list | 1, 2 | 31/12/2018 | 31/12/2019 |
| 4th priority list | 6, 13 | 31/12/2019 | 31/12/2020 |
| 5th priority list | 7, 9, 10 | 31/12/2020 | 31/12/2021 |
| 6th priority list | 11, 12, 15, 17, 22, 23 (new PT20 under BPR) |
31/12/2022 | 31/06/2024 |
Ha a hatóanyag felülvizsgálat sikeresen lezárul, akkor 5, 7. vagy 10 évig fennmaradhat a hatóanyag az elfogadott hatóanyagok listáján.
Hogyan is fogjon hozzá az új biocid rendelet betartásához az a cég, aki EU-n kívülről vásárol biocid terméket, vagyis biocid termék importőr?
A legfontosabb szabály amire figyelnie kell:
2015. szeptember 1-jétől nem hozható forgalomba a biocid termék, amennyiben a benne lévő hatóanyag(ok) gyártója vagy importőre, illetve adott esetben a biocid termék importőre nem szerepel az alábbi listán:
Elfogadott hatóanyagok »
(Az ECHA rendszeresen aktualizálja ezt a listát)
Az első feladat:
- Mivel Önök a biocid termékkel együtt a biocid hatóanyagot is importálják, 2015. szeptember 1-jére fel kell kerülniük az elfogadott hatóanyag listára.
Ha nem kerülnek fel erre a listára, akkor 2015. szeptember 1-vel nem importálhatják a biocid termékeket, és nem is hozhatja az Önök által importált biocid terméket senki sem forgalomba az EU-ban. Tehát van 2 évük, hogy kivezessék a piacról ezt a biocid terméket.
Ha szeretnék, hogy felkerüljenek az elfogadott hatóanyagok listára, akkor az alábbi teendőjük van. - Az R4BP rendszeren keresztül inquiry-t nyújtanak be, hogy megkapják a konkrét elérhetőségét azoknak a cégeknek, akiknek már vannak tesztjeik, és akiktől hozzáférési felhatalmazást (LOA) lehetne szerezni.
Ha inquiry nélkül is meg tudják találni a lista alapján az elérhetőséget az lenne a leggyorsabb megoldás. - Tárgyalnak a hozzáférési felhatalmazás (LOA) áráról vagy
- Saját maguk megcsináltatják / összegyűjtik a teszteket a II és III melléklet követelményei alapján. Ez egy hatalmas munka, tanácsadó nélkül nem fogják tudni megcsinálni.
- Hatóanyag jóváhagyást nyújtanak be.
Hatóanyag jóváhagyás
A biocid hatóanyag gyártójának vagy importőrének be kell adni a hatóság felé a 6. cikk alapján egy hatóanyag jóváhagyási IUCLID dosszié-t a R4BP rendszeren keresztül 2015 szeptember 1-ig, ami alapján felkerül a hatóanyag az elfogadott hatóanyagok listára.
Tartalma:
- a hatóanyagra vonatkozó dokumentációt (II. melléklet) vagy
- a hatóanyagra vonatkozó hozzáférési felhatalmazást (LOA) és
- a biocid termékre vonatkozó dokumentációt (III. melléklet) vagy
- a biocid termékre vonatkozó hozzáférési felhatalmazást (LOA).
- Felülvizsgálati program
A hatóanyagot egy felülvizsgálati programon belül értékeli az EU Bizottsága az alábbi határidőre:
| Priority | Existing active substances for product types |
All draft CARs have to be submitted to ECHA by |
The BPC have to submit all its opinions by |
| 1st priority list | 8, 14, 16, 18, 19, 21 | 31/12/2015 | 31/12/2016 |
| 2nd priority list | 3, 4, 5 | 31/12/2016 | 31/12/2017 |
| 3rd priority list | 1, 2 | 31/12/2018 | 31/12/2019 |
| 4th priority list | 6, 13 | 31/12/2019 | 31/12/2020 |
| 5th priority list | 7, 9, 10 | 31/12/2020 | 31/12/2021 |
| 6th priority list | 11, 12, 15, 17, 22, 23 (new PT20 under BPR) |
31/12/2022 | 31/06/2024 |
Biocid termék engedélyezése
Ha a hatóanyag felülvizsgálat sikeresen lezárul, akkor 5, 7. vagy 10 évig fennmaradhat a hatóanyag az elfogadott hatóanyagok listáján, és 3 éven belül a biocid termék gyártójának illetve az importőrének be kell adni a biocid termékre az engedélyt.
Tehát az 1 termékcsoport esetében 2018 végére lesz meg a felülvizsgálat, és 3 évre rá, 2021-re kell elkészíteni a biocid termék importőrének / gyártójának a biocid termék engedélyt.
A biocid termék engedélyét szintén a IUCLID programmal és az R4BP programmal kell elkészíteni. A 20. cikk alapján csatolni kell hozzá.
- a hatóanyagra vonatkozó dokumentációt (II. melléklet) vagy
- a hatóanyagra vonatkozó hozzáférési felhatalmazást (LOA) és
- a biocid termékre vonatkozó dokumentációt (III. melléklet) vagy
- a biocid termékre vonatkozó hozzáférési felhatalmazást (LOA).
(Mivel a biocid hatóanyag jóváhagyásánál is be kellett adni a biocid termékre vonatkozó dokumentumokat, így olyan, mintha kétszer adnák be ugyanazt a IUCLID dossziét, egyszer a hatóanyag jóváhagyásra és egyszer a biocid termék engedélyezésre pár év különbséggel.)
Az biocid termék engedélykérelmeket a leendő engedélyes vagy képviselője nyújtja be.
A biocid engedélyt egyedi biocid termékre vagy biocid termékcsaládra lehet kiadni.
A biocid engedély lehet:
- uniós engedély (minden tagállamban érvényes, de nagyon drága) vagy
- nemzeti engedély (1 tagállamban érvényes).
A nemzeti engedélyt ki lehet terjeszteni a többi tagállamra is:
- egymást követő kölcsönös elismeréssel vagy (lásd 33. cikk)
- párhuzamos kölcsönös elismeréssel (lásd 34. cikk)
Tehát, ha Magyarországra kapják meg ezt a bioicd engedélyt, akkor bárki vásárolhatja Önöktől ezt a terméket, és utána forgalmazhatják is, a forgalmazónak nem kell külön engedélyt kapni.
Hogyan is fogjon hozzá az új biocid rendelet betartásához az a cég, aki biocid terméket készít az EU-ban?
A legfontosabb szabály amire figyelnie kell már most:
2015. szeptember 1-jétől nem hozható forgalomba a biocid termék, amennyiben a benne lévő hatóanyag(ok) gyártója vagy importőre, illetve adott esetben a biocid termék importőre nem szerepel az alábbi listán:
Elfogadott hatóanyagok »
(Az ECHA rendszeresen aktualizálja ezt a listát)
Az első feladat:
Meg kell tudni, hogy biocid termékük hatóanyagának gyártója illetve importőre 2015. szeptember 1-jére felkerül –e erre a listára?
- Ha nem, akkor 2015. szeptember 1-vel nem hozhatják forgalomba ezeket a biocid termékeket Önök sem, így javaslom, hogy váltsanak hatóanyag beszállítót minél hamarabb.
- Ha igen a válasz, és felkerül a hatóanyag gyártójuk vagy importőrük erre a listára, akkor Önök forgalmazhatják ezt a biocid terméket nyugodtan, de előtte még ellenőrizzék le a terméktípust is, mert a hatóanyag jóváhagyás mindig valamely terméktípusra vonatkozik.
Hatóanyag jóváhagyás
(Ezt nem a biocid termék keverő csinálja, de jó ha érti a folyamatot)
A biocid hatóanyag gyártójának vagy importőrének be kell adni a hatóság felé a 6. cikk alapján egy hatóanyag jóváhagyási IUCLID dosszié-t (ami a teszteket tartalmazza, vagy az azt kiváltó LoA-t mind a hatóanyagra vonatkoztatva mind egy biocid termékre vonatkoztatva) a R4BP rendszeren keresztül 2015 szeptember 1-ig, ami alapján felkerül a hatóanyag az elfogadott hatóanyagok listára.
Ezt követően a hatóanyagot egy felülvizsgálati programon belül értékeli az EU Bizottsága az alábbi határidőre:
| Priority | Existing active substances for product types |
All draft CARs have to be submitted to ECHA by |
The BPC have to submit all its opinions by |
| 1st priority list | 8, 14, 16, 18, 19, 21 | 31/12/2015 | 31/12/2016 |
| 2nd priority list | 3, 4, 5 | 31/12/2016 | 31/12/2017 |
| 3rd priority list | 1, 2 | 31/12/2018 | 31/12/2019 |
| 4th priority list | 6, 13 | 31/12/2019 | 31/12/2020 |
| 5th priority list | 7, 9, 10 | 31/12/2020 | 31/12/2021 |
| 6th priority list | 11, 12, 15, 17, 22, 23 (new PT20 under BPR) |
31/12/2022 | 31/06/2024 |
Biocid termék engedélyezése
(Ezt már a biocid termék keverője csinálja)
Ha a hatóanyag felülvizsgálat sikeresen lezárul, akkor 5, 7. vagy 10 évig fennmaradhat a hatóanyag az elfogadott hatóanyagok listáján, és 3 éven belül a biocid termék gyártójának be kell adni a biocid termékre az engedélyt.
Tehát a táblázatból látható, hogy pl. az 1 termékcsoport esetében 2018 végére lesz meg a felülvizsgálat, és 3 évre rá, 2021-re kell elkészíteni a biocid termék importőrének / gyártójának a biocid termék engedélyt.
A biocid termék engedélyét szintén a IUCLID programmal és az R4BP programmal kell elkészíteni. A 20. cikk alapján csatolni kell hozzá.
- a hatóanyagra vonatkozó dokumentációt (II. melléklet) vagy
- a hatóanyagra vonatkozó hozzáférési felhatalmazást (LOA) és
- a biocid termékre vonatkozó dokumentációt (III. melléklet) vagy
- a biocid termékre vonatkozó hozzáférési felhatalmazást (LOA).
Az engedélykérelmeket a leendő engedélyes vagy képviselője nyújtja be. A biocid engedélyt egyedi biocid termékre vagy biocid termékcsaládra lehet kiadni.
A biocid engedély lehet:
- uniós engedély (minden tagállamban érvényes, de nagyon drága) vagy
- nemzeti engedély (1 tagállamban érvényes).
A nemzeti engedélyt ki lehet terjeszteni a többi tagállamra is:
- egymást követő kölcsönös elismeréssel vagy (lásd 33. cikk)
- párhuzamos kölcsönös elismeréssel (lásd 34. cikk)
Ön mindet leellenőrizte már? Ha nem, tegye meg most!
Ha az Ön számára is vannak ilyen bizonytalanságok, akkor kérem, vegye fel a telefont és kérdezzen meg, vagy írjon egy e-mailt, mert szívesen válaszolok. Nekem, mint REACH, GHS és biocid tanácsadónak sokkal több időm van azzal foglalkozni, hogy mindent elolvassak a biocid rendeletből, valamint az útmutatókból az ügyfél helyett is. Együtt gondolkodva el tudjuk dönteni, hogy mi lenne a legjobb biocid stratégia az Ön cégének, így időt és pénzt tudunk megspórolni a cégének.
Botos Ágnes
A GHS-expert Kft. ügyvezetője
E-mail: agnes.botos@ghsexpert.com
Telefon: +36-20/220-5737
Hogyan is fogjon hozzá az új biocid rendelet betartásához az a cég, aki EU-s beszállítótól vásárolt biocid terméket forgalmaz?
A legfontosabb szabály amire figyelnie kell már most:
2015. szeptember 1-jétől nem hozható forgalomba a biocid termék, amennyiben a benne lévő hatóanyag(ok) gyártója vagy importőre, illetve adott esetben a biocid termék importőre nem szerepel az alábbi listán:
Elfogadott hatóanyagok »
(Az ECHA rendszeresen aktualizálja ezt a listát)
Az első feladat:
Meg kell tudni, hogy biocid termékük hatóanyagának gyártója illetve importőre 2015. szeptember 1-jére felkerül –e erre a listára?
- Ha nem, akkor 2015. szeptember 1-vel nem hozhatják forgalomba ezeket a biocid termékeket Önök sem, így javaslom, hogy ne raktározzanak be belőle sokat.
- Ha igen a válasz, és felkerül a hatóanyag gyártójuk vagy importőrük erre a listára, akkor Önök forgalmazhatják ezt a biocid terméket nyugodtan, de előtte még ellenőrizzék le a terméktípust is, mert a hatóanyag jóváhagyás mindig valamely terméktípusra vonatkozik.
Hatóanyag jóváhagyás
(Ezt nem a forgalmazó csinálja, de jó ha érti a folyamatot)
A biocid hatóanyag gyártójának vagy importőrének be kell adni a hatóság felé a 6. cikk alapján egy hatóanyag jóváhagyási IUCLID dosszié-t (ami a teszteket tartalmazza, vagy az azt kiváltó LoA-t mind a hatóanyagra vonatkoztatva mind egy biocid termékre vonatkoztatva) a R4BP rendszeren keresztül 2015 szeptember 1-ig, ami alapján felkerül a hatóanyag az elfogadott hatóanyagok listára.
Ezt követően a hatóanyagot egy felülvizsgálati programon belül értékeli az EU Bizottsága az alábbi határidőre:
| Priority | Existing active substances for product types |
All draft CARs have to be submitted to ECHA by |
The BPC have to submit all its opinions by |
| 1st priority list | 8, 14, 16, 18, 19, 21 | 31/12/2015 | 31/12/2016 |
| 2nd priority list | 3, 4, 5 | 31/12/2016 | 31/12/2017 |
| 3rd priority list | 1, 2 | 31/12/2018 | 31/12/2019 |
| 4th priority list | 6, 13 | 31/12/2019 | 31/12/2020 |
| 5th priority list | 7, 9, 10 | 31/12/2020 | 31/12/2021 |
| 6th priority list | 11, 12, 15, 17, 22, 23 (new PT20 under BPR) |
31/12/2022 | 31/06/2024 |
Biocid termék engedélyezése
Ha a hatóanyag felülvizsgálat sikeresen lezárul, akkor 5, 7. vagy 10 évig fennmaradhat a hatóanyag az elfogadott hatóanyagok listáján, és 3 éven belül a biocid termék gyártójának illetve az importőrének be kell adni a biocid termékre az engedélyt.
Tehát az 1 termékcsoport esetében 2018 végére lesz meg a felülvizsgálat, és 3 évre rá, 2021-re kell elkészíteni a biocid termék importőrének / gyártójának a biocid termék engedélyt.
A biocid termék engedélyét szintén a IUCLID programmal és az R4BP programmal kell elkészíteni. A 20. cikk alapján csatolni kell hozzá.
- a hatóanyagra vonatkozó dokumentációt (II. melléklet) vagy
- a hatóanyagra vonatkozó hozzáférési felhatalmazást (LOA) és
- a biocid termékre vonatkozó dokumentációt (III. melléklet) vagy
- a biocid termékre vonatkozó hozzáférési felhatalmazást (LOA).
Az engedélykérelmeket a leendő engedélyes vagy képviselője nyújtja be.
A biocid engedélyt egyedi biocid termékre vagy biocid termékcsaládra lehet kiadni.
A biocid engedély lehet:
- uniós engedély (minden tagállamban érvényes, de nagyon drága) vagy
- nemzeti engedély (1 tagállamban érvényes).
A nemzeti engedélyt ki lehet terjeszteni a többi tagállamra is:
- egymást követő kölcsönös elismeréssel vagy (lásd 33. cikk)
- párhuzamos kölcsönös elismeréssel (lásd 34. cikk)









